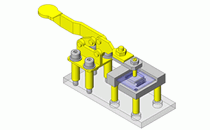
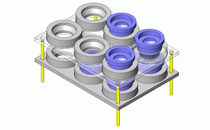
顾名思义,点蚀是指深度远超开口尺寸的腐蚀。这种现象会发生于碳素钢、低合金钢、铜合金、不锈钢、铝合金等金属上,最为众人所知的是发生于不锈钢和铝合金等金属上,这类金属会形成一层具备高耐腐蚀性的钝化膜,但是却会发生点蚀。
点蚀是局部腐蚀以孔状向金属的内表面发展的腐蚀,有时只是偶发,而有时则会多发。在不锈钢等覆盖有钝化膜的表面上,点蚀以外的区域呈光亮发亮的状态。
【图1】中是不锈钢上所发生的点蚀截面的模式图。在之前的讲座中曾经提到,由于不锈钢的表面有一层钝化膜,所以在诸多其他金属中均表现为贵金属特性。
现在,如果一部分钝化膜因氯离子的存在而被破坏,则该部分会因具备低电势而形成负极,周围具有钝化膜的部分会形成正极,从而构成原电池。由于正极部分的面积远大于负极部分,所以腐蚀作用会不断进行下去。
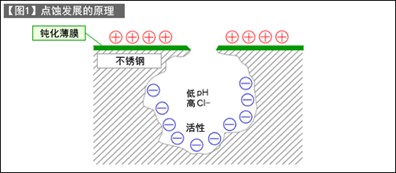
由此,在原电池作用的影响下,点蚀会不断发展。腐蚀电流从作为负极的钝化膜破损部位流出到水中,并从水中流过后进入周边的正极。电流在水中流动并非因为电子迁移,而是因为溶解的离子发生迁移。在电池中,阴离子向负极移动,阳离子向正极移动,从而产生电流。
而不锈钢上发生点蚀的原因在于,当有氯离子 (CL-) 存在的情况下,氯离子在环境中的电流流动中发挥了作用。由于氯离子是负离子,当其聚集在点蚀区域时,该区域的氯浓度增加并在孔中积聚。由此导致pH降低,加快了金属的溶解。随着点蚀的进行,从不锈钢中溶出的金属离子在水中发生水解,从而产生氢离子。
由于氢离子H+和氯离子CL-的聚集现象是发生于腐蚀正在进行的孔隙中,所以它们不易逃逸到外部环境中。从而使得发生点蚀的地方持续不断地腐蚀下去。